Los ácidos nucleicos son macromoléculas, polímeros formados por la repetición de monómeros llamados nucleótidos, unidos mediante enlaces fosfodiéster. Se forman, así, largas cadenas o polinucleótidos, lo que hace que algunas de estas moléculas lleguen a alcanzar tamaños gigantes (de millones de nucleótidos de largo).
El descubrimiento de los ácidos nucleicos se debe a Friedrich Miescher, quien en el año 1869 aisló de los núcleos de las células una sustancia ácida a la que llamó nucleína, nombre que posteriormente se cambió a ácido nucleico.
En la naturaleza existen solo dos tipos de ácidos nucleicos: El ADN (ácido desoxirribonucleico) y el ARN (ácido ribonucleico) y están presentes en todas las células.

FUNCIONES GENERALES
Los ácidos nucleicos, llamados así porque
en un principio fueron localizados en el
núcleo celular, son las moléculas de la
herencia y por lo tanto van a participar en
los mecanismos mediante los cuales la
información genética se almacena, replica y
transcribe. Ésta no va a ser su única
función. Determinados derivados de estas
sustancias: los nucleótidos, van a tener
otras funciones biológicas, entre las que pueden destacarse, como ejemplo, la de
servir de intermediarios en las transferencias de energía en las células (ATP, ADP y
otros) o en las transferencias de electrones (NAD+ , NADP+ , FAD, etc.).
Tipos de ARN
Los productos de la transcripción no son sólo ARNm. Existen varios tipos diferentes de ARN, relacionados con la síntesis de proteínas. Así, existe ARN mensajero (ARNm), ARN ribosómico (ARNr), ARN traductor (ARNt) y un ARN heterogéneo nuclear (ARN Hn).
Dentro del ADN hay genes que codifican para ARNt y ARNr.
ARNHn
ARN heterogéneo nuclear = ARNm primario: localizado en el núcleo y de tamaño variable. Precursor del ARN mensajero, se transforma en él tras la eliminación de los intrones, las secuencias que no codifican genes.
Transcripción o síntesis a ARN
Básicamente, la relación entre el ADN, el ARN y las proteínas se desarrolla como un flujo de actividad celular. Dicho flujo, que hoy constituye el dogma central de la biología molecular, podríamos graficarlo así:
ADN --------> ARN ----------------> PROTEINAS
replicación --> transcripción --> traducción
replicación --> transcripción --> traducción

bibliografia: http://es.wikipedia.org/wiki/%C3%81cido_nucleico

 estructura adenina
estructura adenina estructura timina
estructura timina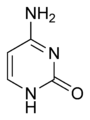 estructura citocina
estructura citocina estructura guanina
estructura guanina estructura uracilo
estructura uracilo